Начну с цитаты учебника биохимии под редакцией Северина [8]: “Молекулы жиров в адипоцитах объединяются в крупные жировые капли, не содержащие воды, и поэтому являются наиболее компактной формой хранения топливных молекул. Подсчитано, что, если бы энергия, запасаемая в жирах, хранилась в форме сильно гидратированных молекул гликогена, то масса тела человека увеличилась бы на 14-15 кг.”
Еще одна вводная цитата: «Механизм переключения режима хранения энергии на режим траты может быть терапевтической целью в борьбе с ожирением» [5].
Термогенез и термогенин [1]
Жир – эффективный способ запасать энергию. Чтобы от жира избавиться, нам нужен способ тратить/рассеивать эту лишнюю энергию. Млекопитающим везет в том, что гомойотермия (постоянная температура тела) дает нам механизм, необходимый для выживания в холодных условиях [2], благодаря которому наши митохондрии могут рассеивать энергию преимущественно из жиров в виде тепла. Так называемый «холодный термогенез» или non-shivering thermogenesis.
Рассеивать энергию может uncoupling protein 1 (UCP1), он же термогенин.
Термогенез бурого жира связывают с термогенином (UCP1), белком внутренней мембраны митохондрий.
UCP1 улучшает проводимость внутренней мембраны для Н+, что рассеивает митохондриальный Н+ градиент. Это означает, что даже при избытке АТФ жиры продолжат «гореть» в митохондриях, при этом полученная энергия будет рассеиваться в виде тепла.
Путь получается примерно таким:
Стресс холода
Норадреналин
Адренергическая стимуляция жировых капель в клетках бурой жировой ткани
Длинноцепочные кислоты из жировой капли клетки стимулируют термогенин
Термогенин (UCP1) рассеивает Н+- градиент
Жиры перерабатываются (даже при избытке АТФ) в тепло.
UCP1 впоследствии ингибируется цитозольными пуриновыми нуклеотидами. Механизм, благодаря которому жирные кислоты это преодолевают, остается неизвестным.
Механизм активации термогенина, естественно, более комплексный. Другие факторы рассмотрим немного позже. Роль свободных жирных кислот в прямой активации (присоединяются) UCP1 показал Андрий Федоренко с коллегами [1].
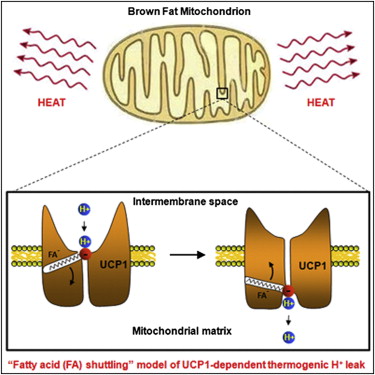
Рисунок 1. Свободная жирная кислота из жировой капли активирует термогенин (UCP1) [1], который приводит рассеиванию энергии в виде тепла.
Возникновение бурого жира в процессе эволюции и его роль [9]
Эндогенная выработка тепла дает млекопитающим ряд эволюционных преимуществ, но значительная часть энергии вынуждена расходоваться на поддержание температуры тела в более холодной среде. Большинство термо-сенсоров в нашем организме реагируют на холод.
Существуют 2 основных механизма реагирования на холод – shivering и non-shivering. Через дрожь, когда холодный стимул заставляет мышцы быстро сокращаться, преобразуя механическую энергию в тепло. И термогенез без сокращений мышц, обусловленной сжиганием жира ради тепла. Этот механизм является более энергоэффективным. В нем участвуют бурый жир и термогенин.
Самые древние следы термогенина относятся к 400 млн лет до н.э. Около 170 млн лет назад однопроходные отделились от ветви развития млекопитающих. В них есть следы UCP1, но UCP1-положительный адипоцитов в них по сей день не обнаружили. У южноамериканского сумчатого обнаружили начальную стадию развития UCP1 мРНК. У астралийской жирнохвостной сумчатой мыши обнаружили подобие бурой жировой ткани, но в ней не было адаптивной функции холод-норадреналировный_стресс-активация_UCP1. У афротерий обнаруживают термогенный бурый жир при низких температурах окружающей среды. У готтентотского златокрота термогенез бурого жира считается основным адаптивным механизмом к холоду. Схематически путь эволюции термогенного бурого жира отражен на рисунке ниже.
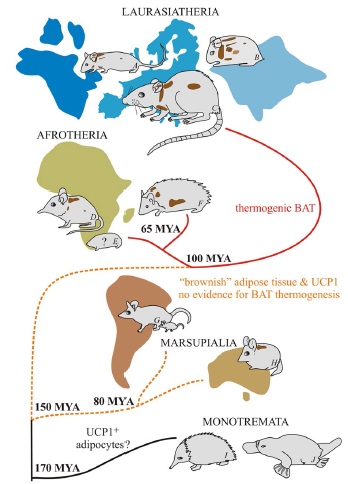
Рисунок 2. Появление термогенного бурого жира, активирующегося на холоде, в процессе эволюции млекопитающих.
Типы жировой ткани [2, 3]
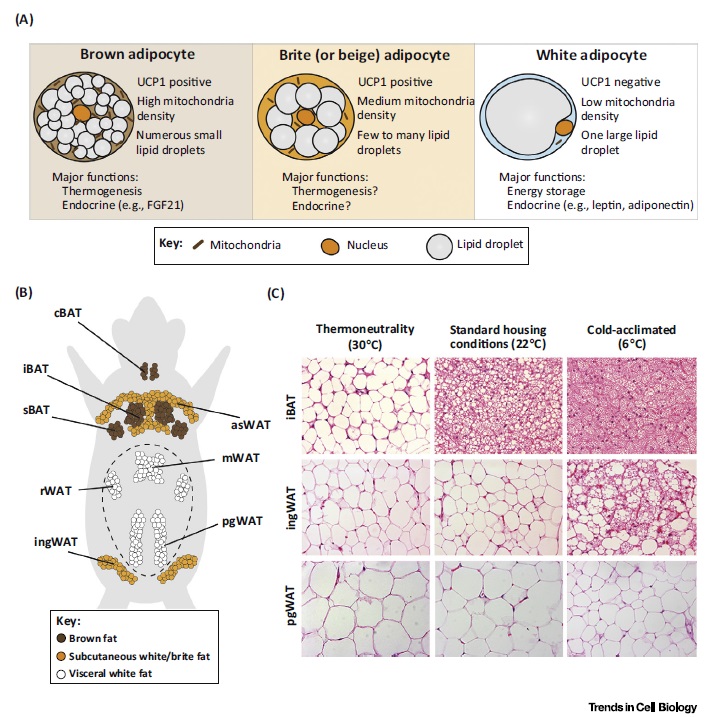
Рисунок 3. Типы жировой ткани и ее пластичность в ответе на температурные изменения. A) Основные морфологические и функциональные различия между бурыми, бежевыми и белыми адипоцитами. В) Анатомической расположение основных отложений жировой ткани. Бурый: iBAT – межлопаточный бурый; sBAT – подлопаточный бурый; cBAT – шейный; Подкожный белый: asWAT – передний подкожный белый; ingWAT – паховый; висцеральный жир: mWAT – брыжеечный; rWAT – забрюшинный; pgWAT - perigonadal. Пунктир – брюшина. С) Модель бурого/белого жира в C57BL6 мышах-самцах возраста 13 недель. В термонейтральной зоне (30 градусов, 4 недели) бурые адипоциты стали напоминать белый. С 22 градусов бурый жир стал активным. При прогрессивном понижении температуры с 22 до 6 градусов подкожный белый жир изменяется и начинает напоминать бурый. Висцеральный жир в целом устойчив к температурным воздействиям.
Бурая жировая ткань (BAT)
Бурую жировую ткань отличает большое количество митохондрий, большое количество небольших жировых капель и большая выраженность разобщающего белка 1 (UCP1). Без внешней стимуляции бурый жир менее активен из-за пуриновых нуклеотидов. Холодный стресс приводит как к активации UCP1, так и к липолизу, предоставляющему топливо для нужд термогенеза. Активный бурый жир импортирует глюкозу и жирные кислоты, чтобы предоставить дополнительное топливо для поддержания термогенеза.
У людей и мышей бурые адипоциты концентрируются в местах большого притока крови. Самые большие отложения в межлопаточной, подлопаточной и шейной зонах. Небольшие запасы в районе почечного рубчика, аорты. Посмертный анализ людей показал, что отложения бурого жира есть вокруг сонной артерии. До 2007 года наука отрицала наличие бурого жира у взрослого человека. Есть обратная корреляция между количеством/активностью бурого жира и индексом массы тела (BMI).
BAT (brown adipose tissue) можем расширяться за счет числа клеток (гиперплазия) и за счет размера клеток (гипертрофия). Гипертрофия во многом зависит от среды. Без температурного стресса бурый жир менее метаболически активен и собирает жиры в одной жировой капле. Но даже при небольшом понижении температуры имеет более привычную многокамерную морфологию жировых капель. Холод уменьшает размер BAT за счет липолиза и бета-оксидации, но продолжительное воздействие холода может увеличить массу бурого жира за счет активации механизмов пролиферации и дифференциации прекурсоров адипоцитов, то есть увеличивая число адипоцитов.
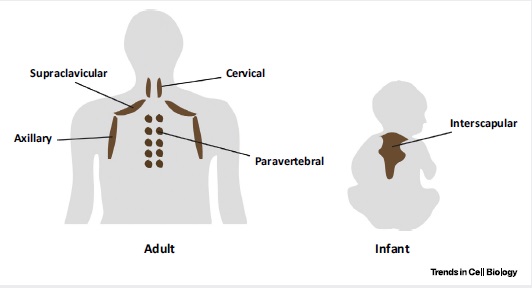
Рисунок 4. Распределение бурой жировой ткани у взрослых (слева) и младенцев (справа)
Белая жировая ткань (WAT)
Белый жир – самый распространенный тип адипоцитов, содержащий одну большую жировую каплю. Основная функция белых адипоцитов – запасать «топливо» и высвобождать адипокины (такие как лептин, адипонектин) для регуляции энергетического гомеостаза. Расширение белого жира (в том числе при ожирении) предохраняет органы и мышцы от липотоксичности. WAT обычно делят на подкожный и висцеральный.
Переизбыток последнего связывают связывают с метаболическими болезнями, в том время как избыток подкожного считают защитным. Белый жир может расширяться как в размере клеток, так и в количестве.
Основные места отложения подкожного и висцерального белого жира отмечены на рисунке 3.
Бежевый жир (brite, brown-in-white)
Есть некая дискуссия о происхождении бежевого жира. Является ли это формой белого жира или это совершенного другая форма жира, активирующаяся при внешнем стимуле – это важно с фармацевтической точки зрения, но не с практической.
«Коричневение» происходит во время энергетического стресса. Наш самый очевидный пример – закаливание, когда энергии от сокращения мышц (дрожи) не хватает для поддержки температуры тела. Но коричневение происходит также и при других внешних стрессах: раковая кахексия, серьезные ожоги, физические упражнения и так далее.
По указанной выше цепочке активируется термогенин (UCP1). Клетки начинают запасать жир и сжигать его для производства тепла. Появляется больше митохондрий и становится больше жировых капель. Висцеральный жир гораздо хуже подвергается «коричневению», чем подкожный белый.
Круговорот жиров [2, 3, 6]
Важно понимать, что именно при воздействии стресса (допустим, холода) бурый жир становится термогенным, белый жир превращается в бежевый (брайт). В отсутствии стимула бурый и бежевый жир начинают напоминать белый.
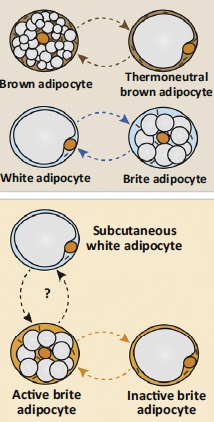
Рисунки 5. Конверсии видов жира друг в друга при наличии/отсутствии внешнего стимула (в частности холода).
Факторы, влияющие на активацию бурого и бежевого жира [2, 3, 7, 12, 13, 14]
Эндогенные факторы, связанные непосредственного с холодом

Рисунок 6. Эндогенные факторы, влияющие на активацию бурого/бежевого жира. Нейроны и макрофаги выделяют ноадреналин; сердце выделяют натрийуретические пептиды; печень и буржый жир выделяют FGF21; мышцы выделяют ирисин; щитовидка Т4, который конвертируется в Т3; бурый жир выделяет bmp8b и vegf, который усиливает термогенную функцию в автокринной манере. Орексин и Bmp7 способствуют образованию бурого жира, хотя их клеточный источник неизвестен;
Эти и другие факторы важны скорее для исследователей, ищущих способы фармацевтической активации бурого жира. Испытания β3-AR агонистов пока не принесли ожидаемого результата на людях. Для нас важнейшим активатором остается холод, который кроме всего прочего способствует росту кровяных сосудов в жировой ткани, что способствует доставке кислорода и термообмену.
Для дальнейшей работы с литературой неплохо запомнить транскрипторный коактиватор PCG-1α, который напрямую связан с биогенезом митохондрий и является центральным транскрипторным эффектором адренергической (стрессовой) активации термогенных адипоцитов.
PPAR-γ рецепторы, которые играют роль в адипогенном механизме.
FGF21 фактор будет встречаться в литературе по метаболическому здоровью (в частности по диабету), этот фактор влияет на улучшение чувствительности инсулину, поглощение глюкозы периферийными клетками, снижает вес.
Найтрийуретические пептиды снижают объем крови, давление, способствуют выделению натрия почками, способствуют липолизу. Логично предположить, что между кардиомиоцитами и жировой тканью должен быть диалог для защиты сердечной мышцы во время холода.
Сильно озабоченным стоит погуглить факторы KLF11, PRDM16, EBF2, ось EWS/YBX1/BMP7, IRF4, ZFP516 или почитать о них по ссылке ниже [14].
Все вышеописанные факторы модулируются холодом, а также фармакологическим вмешательством. Поэтому с практической точки зрения на них не стоит тратить слишком много времени.
Экзогенные факторы, хорошо дополняющие холод [10, 11, 13]
Симпатическая стимуляция β3-адренергических рецепторов больше важна для преобразования белого жира в бежевый (или активации бежевого), чем для бурого.
- Капсаицин (жгучий перец) – стимуляция β3-AR;
- Рыбий жир (омега-3);
- Физические нагрузки;
- Высокожировая диета.
Острый перец и нагрузки – это дополнительный стресс, с этим на уровне формальной логики все ясно.
Ким и коллеги [10] пишут, что рыбий жир активирует симпатическую нервную систему, увеличивает потребление кислорода (читайте оксидацию жиров) и ректальную температуру с активацией β3-AR и термогенина (UCP1). Как любитель мяса хочу заметить, что жиры говядины травяного (читайте ДГК, омега-3) откорма и зернового (омега-6, ненасыщенные жирные кислоты) очень сильно отличаются не только на вкус, но и цвет. При травяном откорме жир бурый, при этом от текстурно хоть и не такой нежный, как его менее здоровый собрат, но значительно вкуснее. Жир же зернового откорма белый.
Цин и коллеги [11] заходят еще дальше и показывают, что бурый (но не белый) жир сам синтезирует ДГК.
Фармацевтические экзогенные средства я не хочу рассматривать по двум причинам: научная сторона пока не пришла к гарантированно рабочим решениям и есть проверенные и действенные средства, не требующие фарм-поддержки.
Кетогенная диета и бурый жир [15, 16]
Сривастава и коллеги [15] опубликовали исследование, в результате которого оказалось, что кетогенная диета способствует активации термогенина в буром жире.
Они взяли 2 группы восьминедельных C57BL/6J мышей. Одну группу кормили NIH-31 диетой (в основном злаки). Другую группу кормили кетогенной диетой с добавлением кетоновых эфиров. Через 3 недели:
- Митохондрии на кето-диете были ближе к жировым каплям;
- Митохондрии на кето-диете были больше и иногда странной формы (тут важно заметить, что это не было отеком митохондрий, а их слиянием – то есть без потери функций);
- В кето-группе было больше жировых капель в клетке, и они были меньше;
- Концентрация циклического АМФ была больше в кето-группе (свидетельствует об усиленном липолизе);
- В кето-группе снизился уровень лептина (то есть смесь кето+закаливание (привет Джеку Крузу, который это первый стал яро пропагандировать) восстанавливает чувствительность лептину);
- Уровень термогенина был выше в кето-группе (таким образом кето-диета способствует активации бурого жира).
Это исследование я в принципе советую пролистать, так как с академической точки зрения оно очень правильно, красиво и хорошо составлено.
Короткое изложение сказанного выше
Холод запускает процесс переработки жиров на тепло. За это в нашем организме отвечает бурый жир, который активирует термогенин (UCP1).
Эта особенность позволяет млекопитающим поддерживать температуру тела в холодной среде.
Холод – норадреналин – жирные кислоты высвобождаются из жировой капли – активация термогенина – сжигание жира ради тепла. Реакция организма на холод более комплексная, но это основной механизм действия.
Бурый жир – это много митохондрий (потому и бурый) и много мелких жировых капель, белый жир – это 1 большая жировая капля и мало митохондрий. Бурый жир не становится белым, белый не становится бурым.
Белый может стать бежевым при закалке и тоже приобрести возможность генерации тепла с морфологическими изменениями в сторону бурого жира (больше митохондрий, больше жировых капель).
Висцеральный белый жир гораздо хуже подкожного поддается «коричневению».
Способствуют образованию/активации бурого жира – капсиацин, рыбий жир, физическая нагрузка, кетогенная диета.
Кето-диета и закаливание отлично дополняют друг друга, улучшая метаболический профиль.
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3782081/
- https://www.ncbi.nlm.nih.gov/pubmed/24100998
- https://www.ncbi.nlm.nih.gov/pubmed/26874575
- https://www.ncbi.nlm.nih.gov/pubmed/25389910
- Turning White Fat into Good Fat
- http://www.nature.com/nrendo/journal....2016.159.html
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3410936/
- Биохимия
- https://www.ncbi.nlm.nih.gov/pubmed/25966796
- http://www.nature.com/articles/srep18013 -
- https://www.ncbi.nlm.nih.gov/pubmed/26802938
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4662916/
- https://www.ncbi.nlm.nih.gov/pubmed/23246573
- https://www.ncbi.nlm.nih.gov/pubmed/26050669
- https://www.ncbi.nlm.nih.gov/pubmed/23233333
- https://www.ncbi.nlm.nih.gov/pubmed/23909803


 LinkBack URL
LinkBack URL About LinkBacks
About LinkBacks








 Ответить с цитированием
Ответить с цитированием





Социальные закладки